大家好,欢迎来到IT知识分享网。
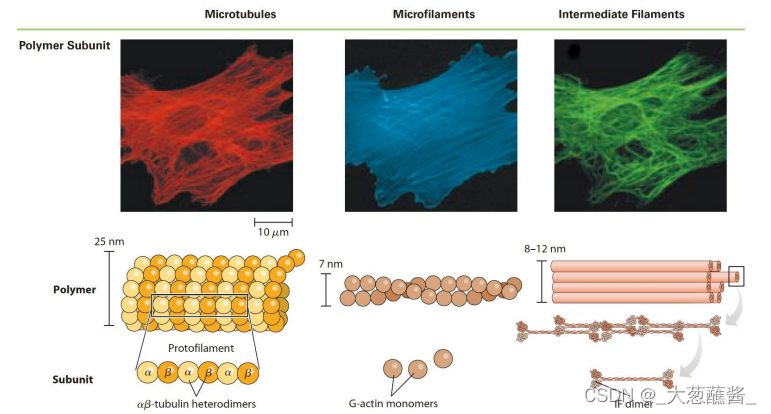
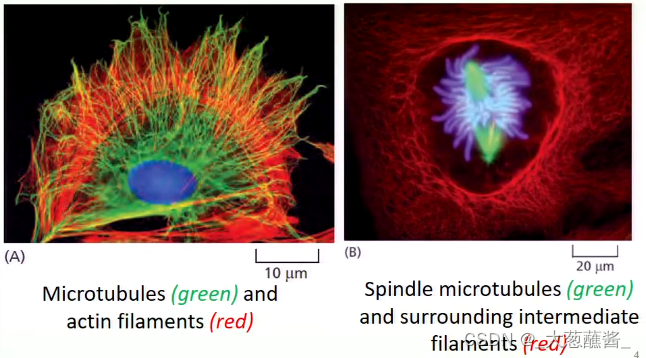
Eukaryotes Have Three Basic Types of Cytoskeletal Elements(微管、微丝、中间纤维)
Bacteria Have Cytoskeletal Systems
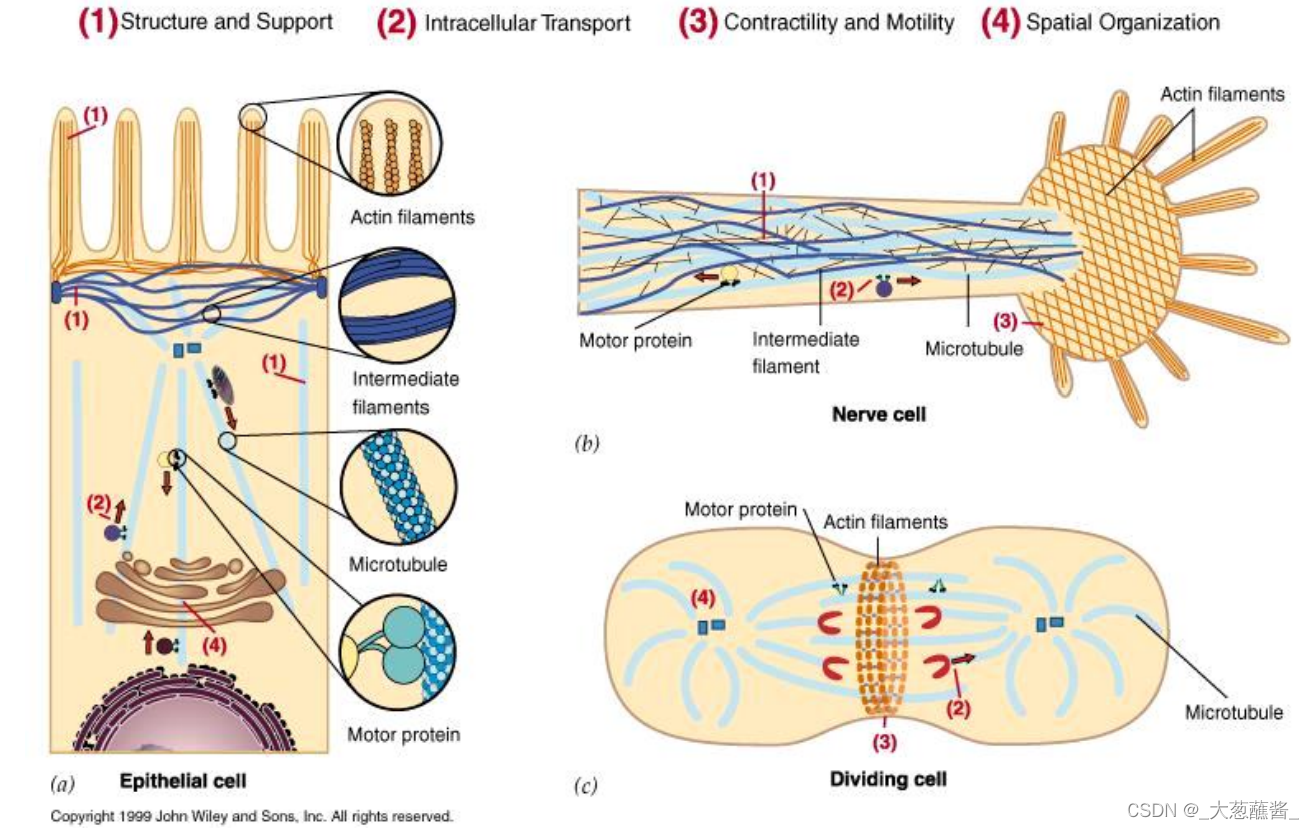
Key to Cytoskeletal Functions
目录
ATP帽(ATP Cap)与踏车行为(treadmilling)
1. Ⅱ型肌球蛋白:传统的肌球蛋白(conventional myosin)
2. 其他类型的肌球蛋白(unconventional myosin)
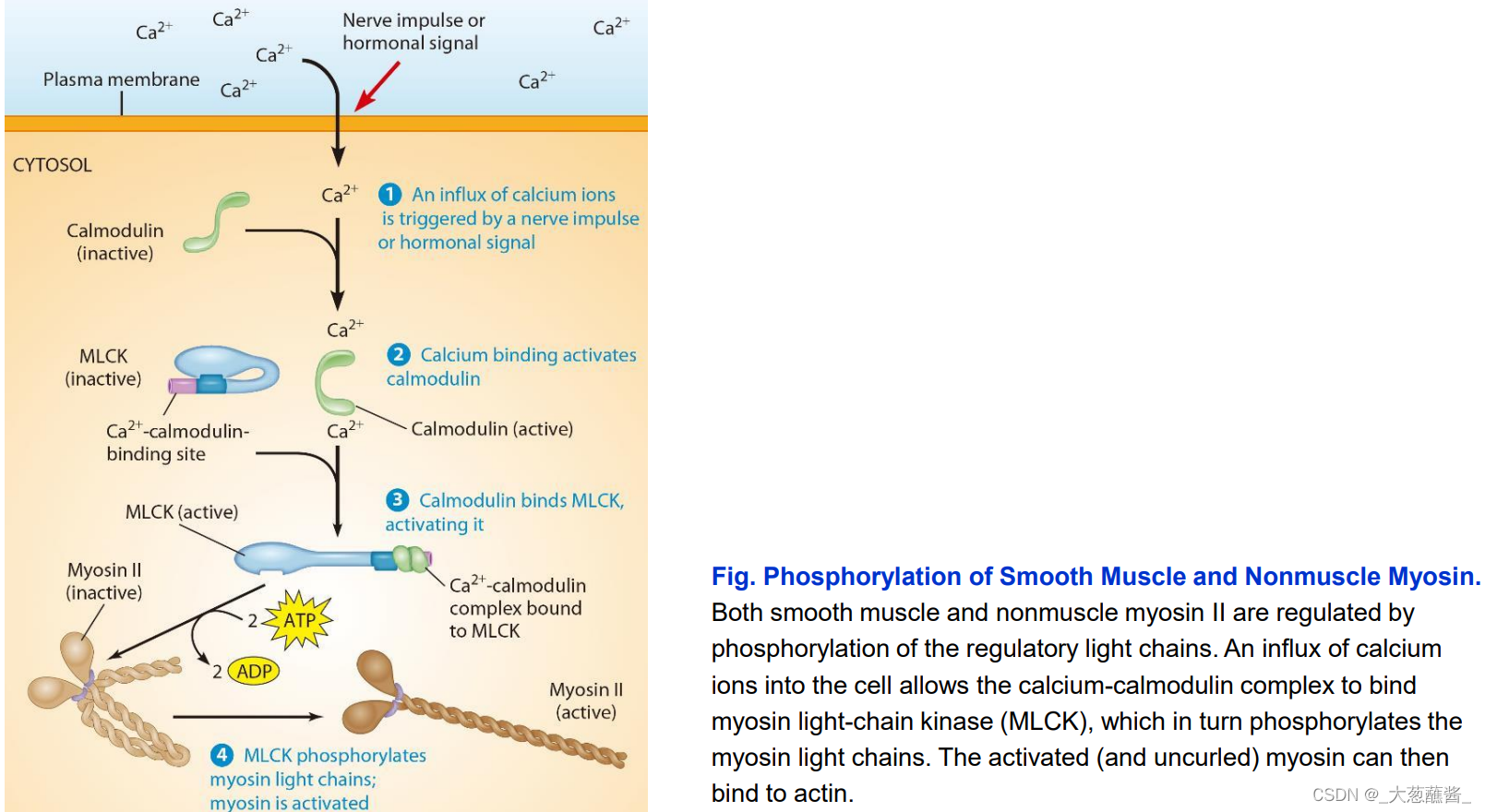
Phosphorylation of myosin II by myosin light-chain kinase (MLCK)
Movement of pigment granules: color adjustment
中间丝又称中间纤维(intermediate filament,IF)
单纯性疱性表皮松懈症(simplex epidermolysis bullosa)
0.细胞骨架的基本概念
细胞骨架(cytoskeleton)一般指真核细胞细胞质内由蛋白质组成的复杂纤维状网架结构体系,包括:微丝、微管、中间纤维。
广义的细胞骨架还包括核骨架和膜骨架。
细胞骨架是高度动态的结构体系,对细胞的结构和功能发挥组织作用,并进一步影响细胞的形态、运动、胞内物质运输及周围的细胞和环境。
第一节 微丝与细胞运动
微丝(microfilament, MF)
微丝又称作肌动蛋白丝(actin filament)或纤维状肌动蛋白(fibrous actin ,F-actin)
直径7 nm;存在于所有的真核细胞中;组装/去组装与多种细胞生命活动密切相关。
肌动蛋白(actin)由一条多肽链构成的球形蛋白质,是组成微丝的基本蛋白质,分子量为43kDa,序列
Eukaryotes Have Three Basic Types of Cytoskeletal Elements(微管、微丝、中间纤维)
Bacteria Have Cytoskeletal Systems
Key to Cytoskeletal Functions
0.细胞骨架的基本概念
细胞骨架(cytoskeleton)一般指真核细胞细胞质内由蛋白质组成的复杂纤维状网架结构体系,包括:微丝、微管、中间纤维。
广义的细胞骨架还包括核骨架和膜骨架。
细胞骨架是高度动态的结构体系,对细胞的结构和功能发挥组织作用,并进一步影响细胞的形态、运动、胞内物质运输及周围的细胞和环境。
第一节 微丝与细胞运动
微丝(microfilament, MF)
微丝又称作肌动蛋白丝(actin filament)或纤维状肌动蛋白(fibrous actin ,F-actin)
直径7 nm;存在于所有的真核细胞中;组装/去组装与多种细胞生命活动密切相关。
肌动蛋白(actin)由一条多肽链构成的球形蛋白质,是组成微丝的基本蛋白质,分子量为43kDa,序列高度保守,具有组织和表达阶段的特异性。存在ATP/ADP结合位点;
α- 肌动蛋白为横纹肌、心肌、血管平滑肌和肠道平滑肌所特有;
β- 肌动蛋白和 γ-肌动蛋白存在于所有的细胞中
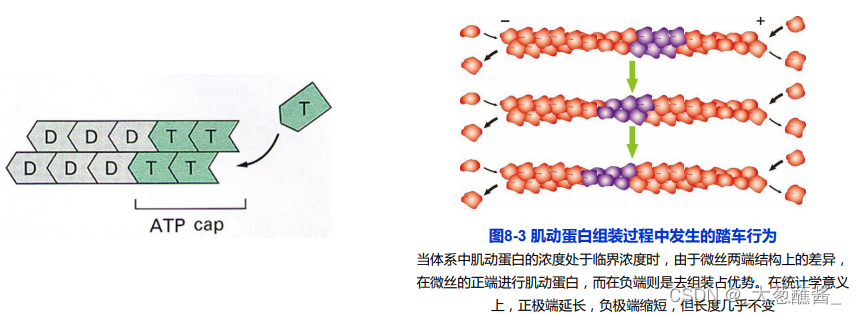
ATP帽(ATP Cap)与踏车行为(treadmilling)
当微丝末端聚合速度大于ATP水解速度时,会在末端形成一个ATP帽;
踏车行为:在体外组装过程中,微丝正极由于肌动蛋白亚基不断增长而延长,负极由于肌动蛋白亚基去组装而缩短的现象。
微丝细胞内组装:受微丝结合蛋白影响
(三)影响微丝组装的特异性药物
细胞松弛素(cytochalasin)
- 与微丝结合之后将微丝切断,并结合在微丝末端阻碍肌动蛋白的聚合,但对微丝解聚没有影响;
- 破坏微丝网络结构,并阻止细胞的运动。
鬼笔环肽(phalloidin)
- 与微丝表面有强亲和力,不与肌动蛋白单体结合;
- 阻止微丝的解聚,使其保持稳定状态。
二、微丝网络结构的调节与细胞运动
细胞中大多数微丝结构处于动态的组装和去组装过程,并通过这种方式实现功能。
(一)非肌肉细胞内微丝的结合蛋白
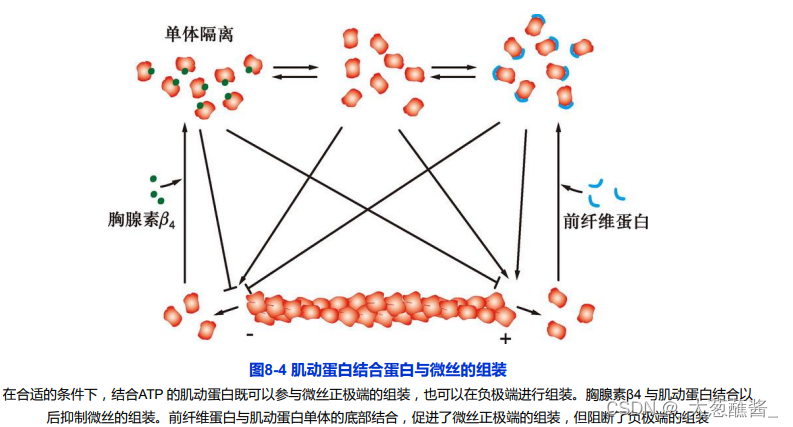
1.肌动蛋白单体结合蛋白
结合ATP的肌动蛋白既可以参与微丝正极端的组装,也可以在负极端进行组装。胸腺素β4与肌动蛋白结合以后抑制微丝的组装。前纤维蛋白与肌动蛋白单体的底部结合,促进了微丝正极端的组装,但阻断了负极端的组装。
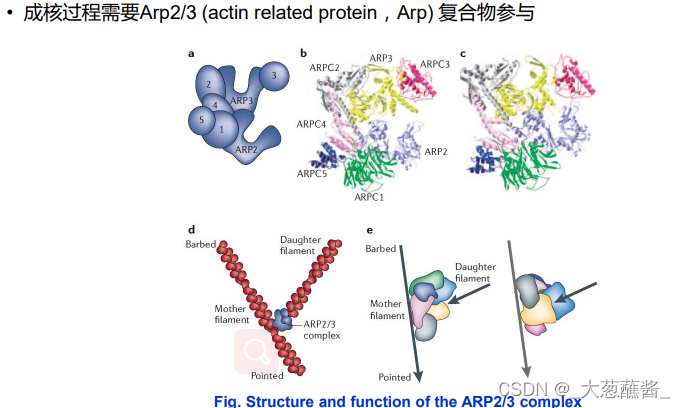
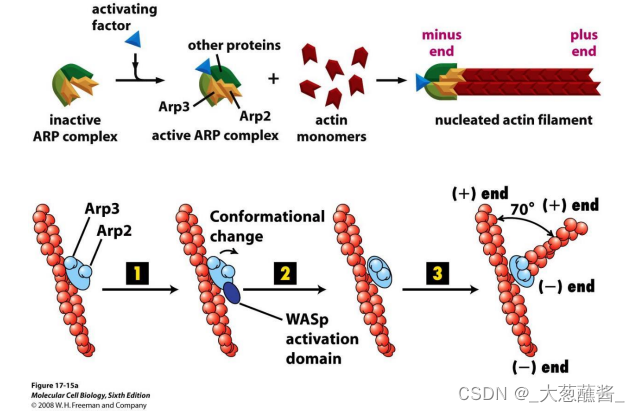
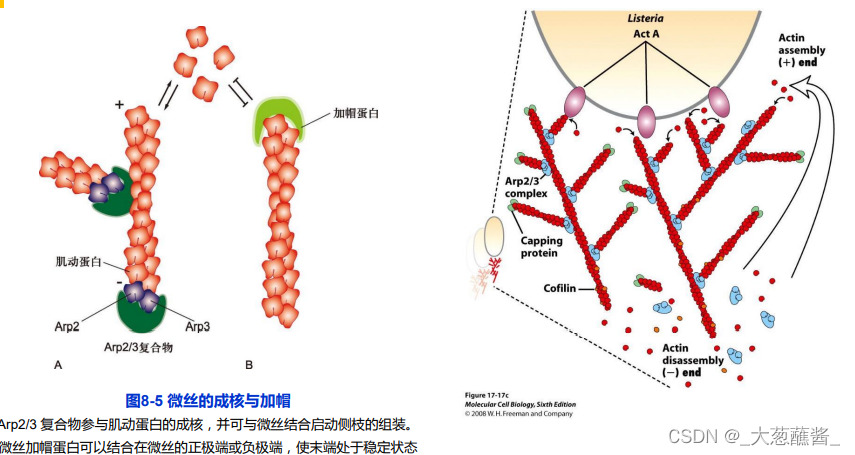
2. 成核蛋白-Arp2/3促进微丝蛋白的分叉
3. 加帽蛋白(capping protein)-增加稳定性
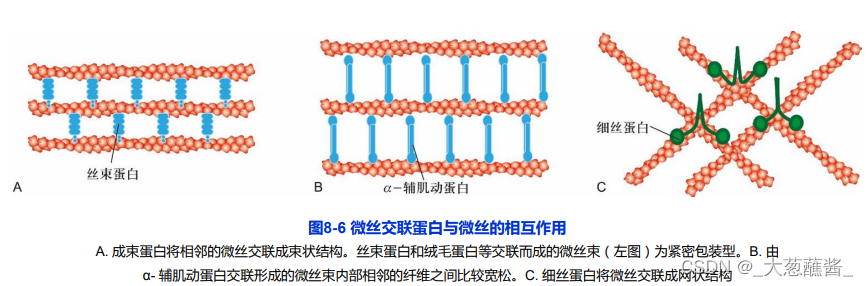
4. 交联蛋白
- 成束蛋白(bunding protein):将相邻的微丝交联成平行排列状态;
- 凝胶形成蛋白(gel-forming protein):将微丝联接成网状。
5. 割断及解聚蛋白
- 凝溶胶蛋白(gelsolin):在高Ca2+(>1 μmol/L)情况下 能将较长微丝切断,使肌动蛋白由凝胶态转化成溶胶态
- 丝切蛋白/ 肌动蛋白解聚因子(cofilin/actin depolymerizing factor,Cofilin/ADF):能与游离的肌动 蛋白或微丝结合,提高微丝的解聚速度
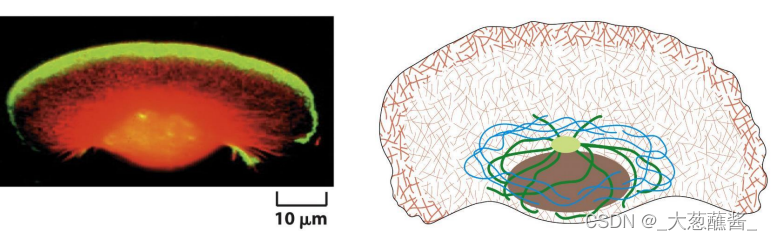
(二)细胞皮层(cell cortex)
细胞内大部分微丝都集中在紧贴细胞质膜的细胞质区域,并由微丝交联蛋白交联成凝胶态的三维网络结构。
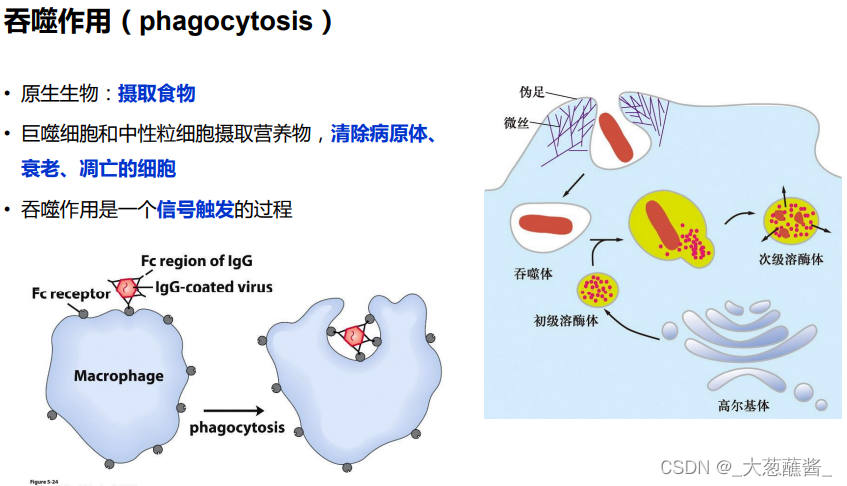
限制膜蛋白的流动性;为细胞质膜提供强度和韧性;维持细胞形状;细胞的多种运动,如胞质环流(cyclosis)、阿米巴运动(amoiboid)、变皱膜运动 (ruffled membrane locomotion)、 吞噬(phagocytosis)以及膜蛋白的定位等与皮层内肌动蛋白的溶胶态- 凝胶态转化相关。
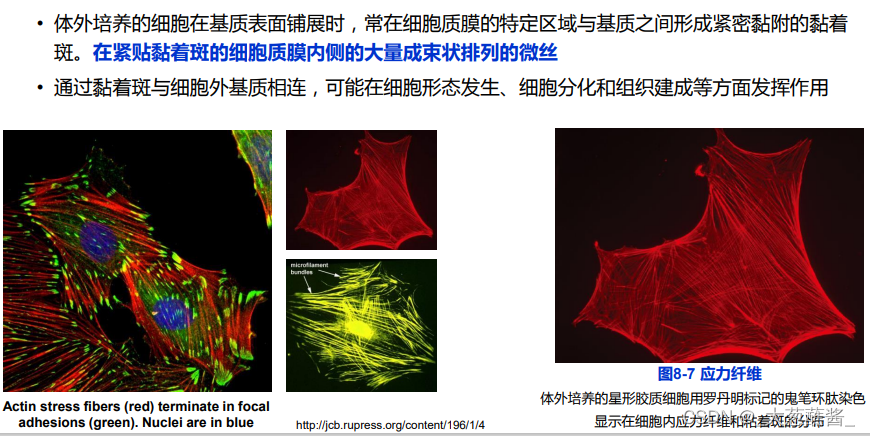
(三)应力纤维
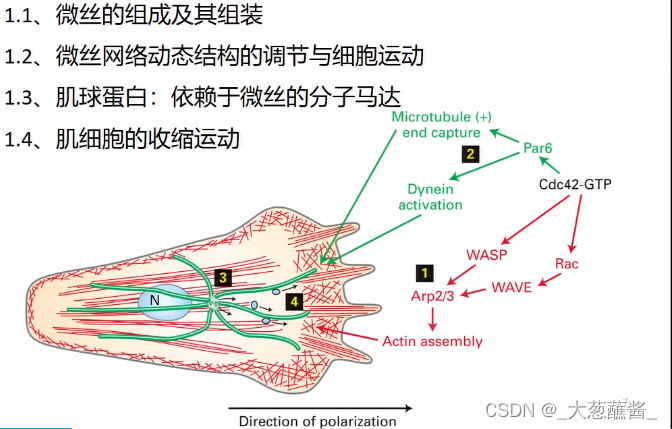
(四)细胞伪足的形成与细胞迁移
三、肌球蛋白:依赖于微丝的分子马达
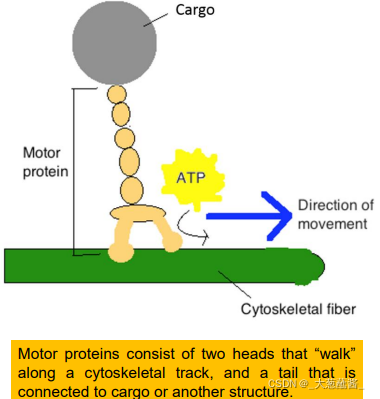
马达蛋白可分为三种:
- 沿微丝运动的肌球蛋白(myosin);
- 沿微管移动的驱动蛋白(kinesin);
- 沿微管移动的动力蛋白(dynein);
马达结构域与微丝或微管结合;货物结合结构域与膜性细胞器或大分子复合物特异性结合;
能量转换:利用水解ATP所提供的能量沿微丝或微管运动。
(一)肌球蛋白的种类
- 骨骼肌细胞内,多个Ⅱ型肌球蛋白分子组装成肌原纤维的粗肌丝;
- 马达结构域是肌球蛋白超家族成员最保守的部位,是肌球蛋白定性和分类的依据;
- 基于马达结构域多肽链一级结构的相似性,至少可以将肌球蛋白超家族成员分成18种家族;
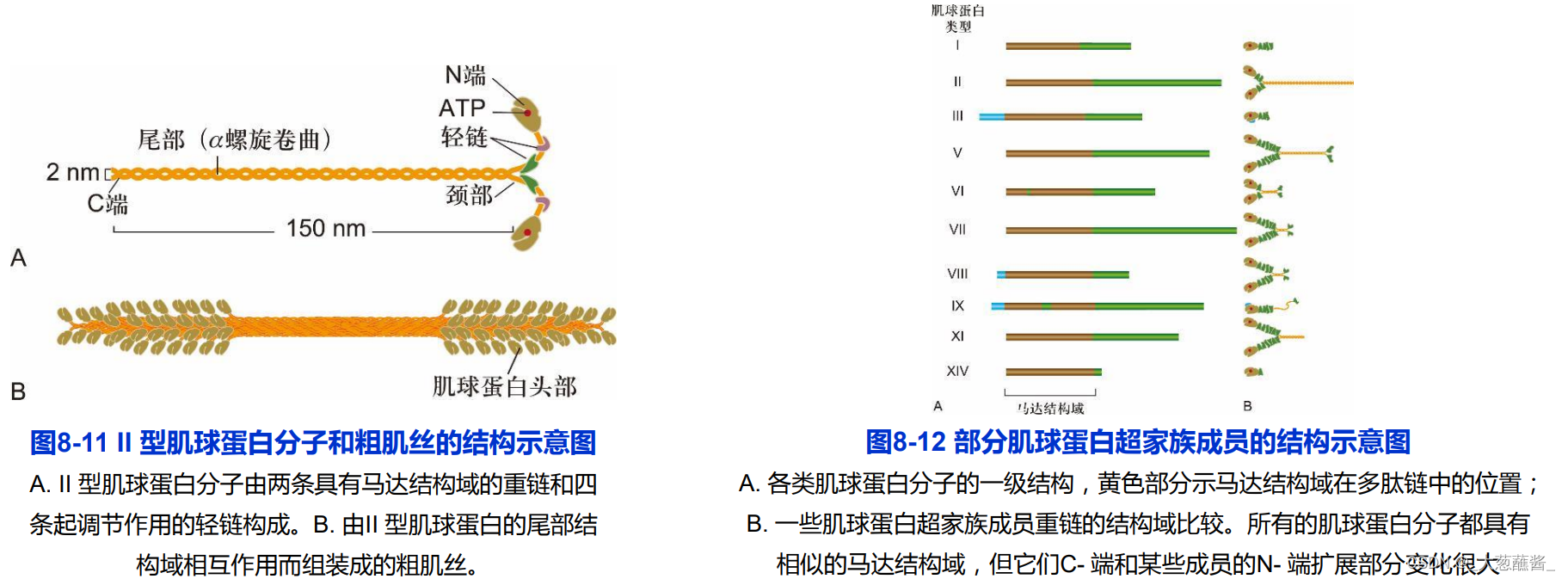
(二)肌球蛋白的结构
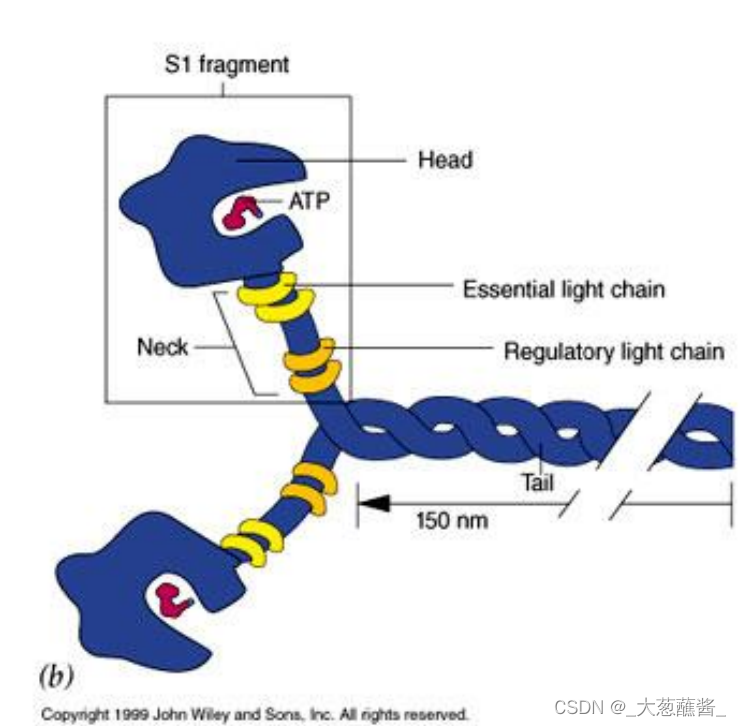
肌球蛋白是沿着微丝运动的马达蛋白,通常有三个功能结构域;
- 马达结构域:位于肌球蛋白的头部,包含一个肌动蛋白亚基结合位点和一个具有ATP酶活性的ATP结合位点,负责将ATP水解释放发化学能转变为机械能。
- 调控结构域:连接马达结构域和尾部杆状区的一段α螺旋,轻链的结合部位,发挥杠杆作用。
- 尾部结构域:选择性与所运输的“货物”结合;
1. Ⅱ型肌球蛋白:传统的肌球蛋白(conventional myosin)
- 肌细胞:组装成肌原纤维的粗丝;
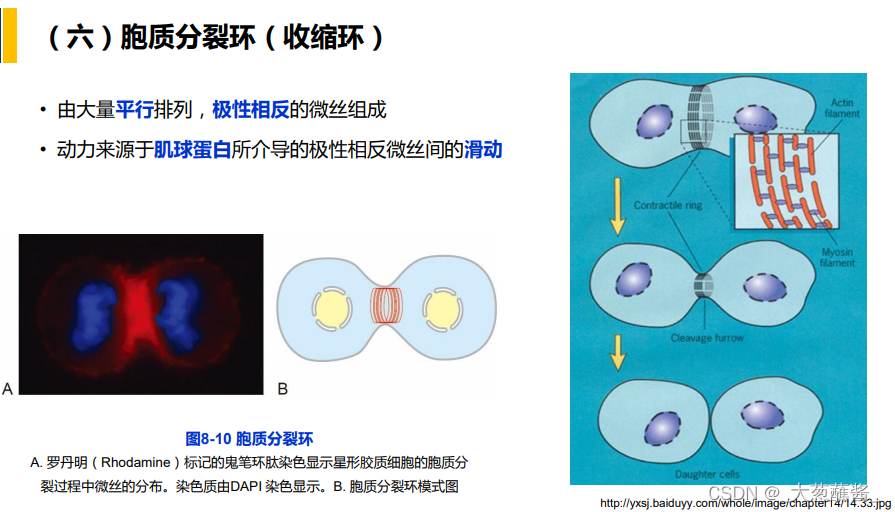
- 非肌细胞:胞质分裂过程中收缩环的主要结构成分;应力纤维的结构成分;
- 包含两条重链和4条轻链,形成一个高度不对称的结构。
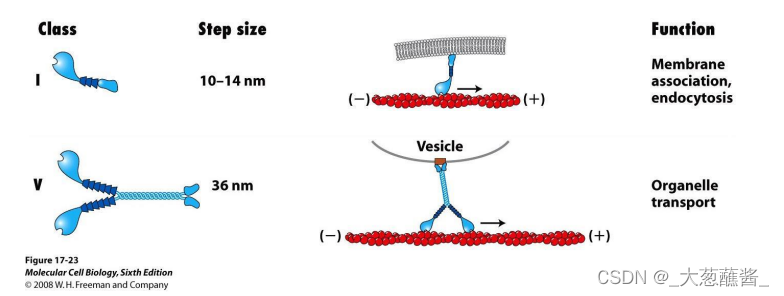
2. 其他类型的肌球蛋白(unconventional myosin)
- Ⅰ型肌球蛋白分子:一个头部(马达结构域)和一个尾部
- Ⅴ型肌球蛋白分子:两条肽链组成的二聚体;两个头部交替与微丝结合
四、肌细胞的收缩运动
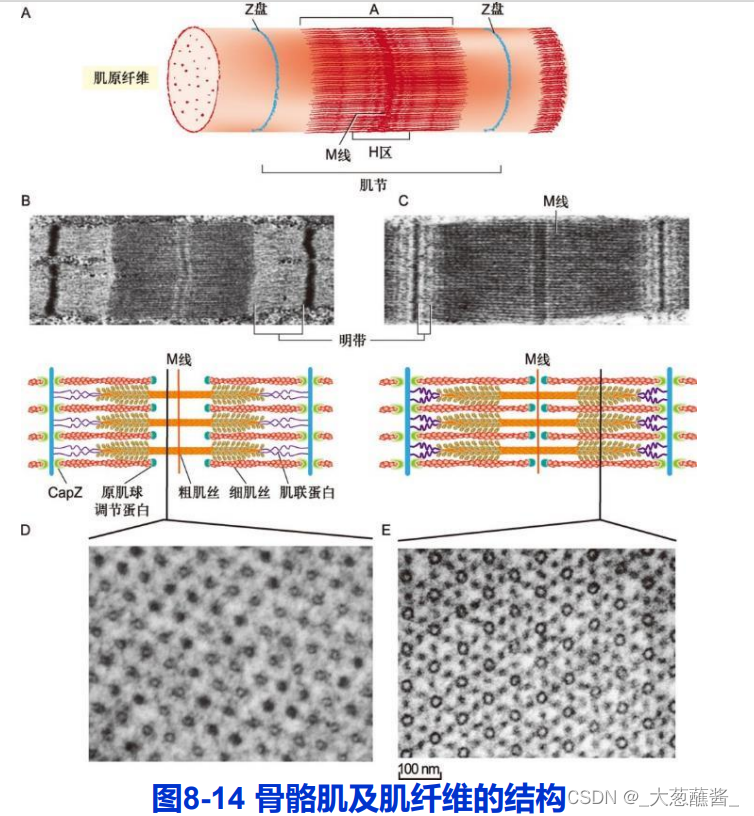
(一)肌纤维的结构
- 肌纤维:肌原纤维(myofibrils);
- 肌节(sarcomere);
- 粗肌丝;细肌丝;
- 横桥;
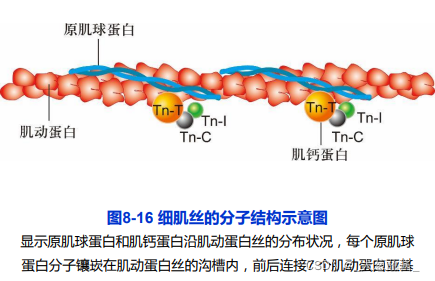
细肌丝结构
肌动蛋白;
- 原肌球蛋白(tropomyosin,Tm);
- 两条平行多肽形成α螺旋构型,调节actin与myosin头部结合;
肌钙蛋白(troponin,Tn):
Tn-C与Ca2+结合;
- Tn-T与原肌球蛋白有高度亲和力;
- Tn-I抑制肌球蛋白马达结构域的ATP酶活性;
肌肉收缩系统中的其他蛋白组分
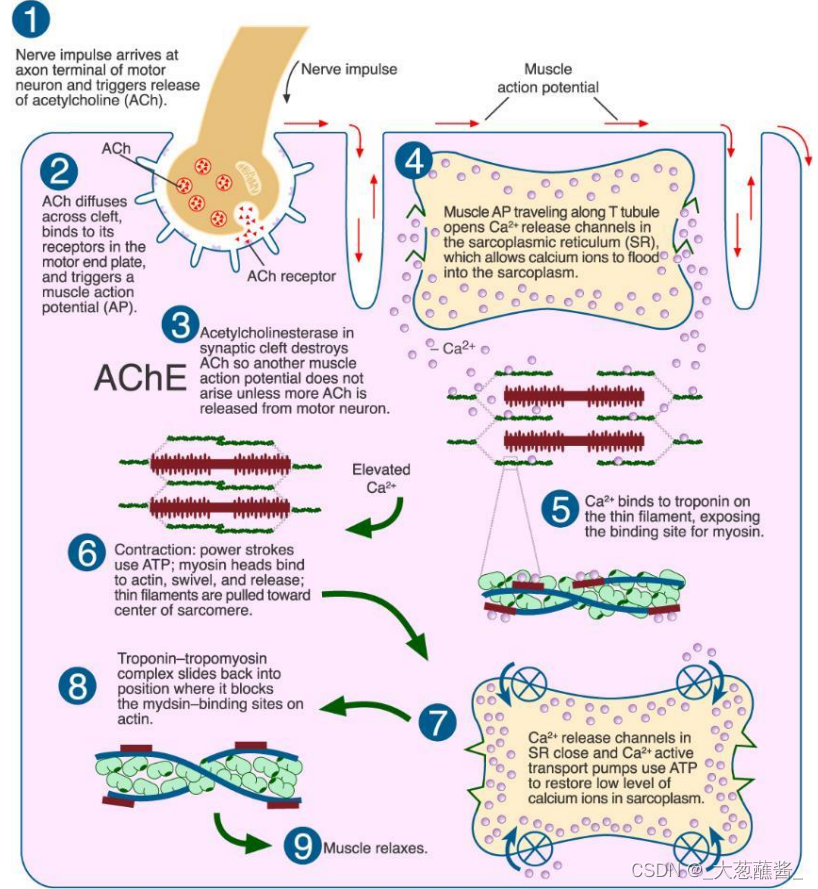
(二)肌肉收缩的滑动模型
肌肉收缩的基本过程:
- 动作电位的产生;
- Ca2+的释放;
- 原肌球蛋白位移;
- 细肌丝和粗肌丝之间的相对滑动;
滑行学说(sliding theory)
Phosphorylation of myosin II by myosin light-chain kinase (MLCK)
第二节 微管及功能
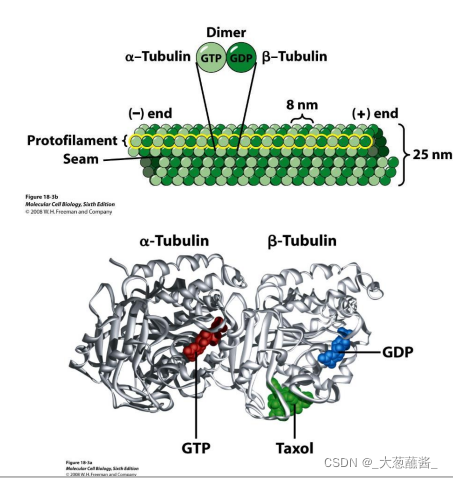
一、微管的结构组成与极性
基本结构:α,β-微管蛋白二聚体;(细胞内游离态微管蛋白的主要存在形式)
GTP结合位点:
- 不可交换位点:α-微管蛋白;
- 可交换位点:β-微管蛋白;
二价阳离子结合位点;
秋水仙素结合位点;
长春花碱结合位点;
13根原纤丝(protofilament)合拢形成微管的管壁;
极性:
- α-微管蛋白所在的一端为(-);
- β-微管蛋白所在一端为(+);
α/β-微管蛋白首先组装成原纤丝;原纤丝侧向相互作用形成片层;由13根原纤丝合拢形成的微管,α/β-微管蛋白从两端加入(或解聚)使微管延长(或缩短)。当体系中α/β-微管蛋白的浓度处于临界浓度时,微管蛋白在微管的正极端组装的速度与负极端去组装的速度相等,微管的长度可以保持不变。
细胞内微管的3种类型
- 单管:细胞质微管或纺锤体微管;
- 二联管:纤毛或鞭毛中的轴丝微管;
- 三联管:中心体或基体中的微管;
免责声明:本站所有文章内容,图片,视频等均是来源于用户投稿和互联网及文摘转载整编而成,不代表本站观点,不承担相关法律责任。其著作权各归其原作者或其出版社所有。如发现本站有涉嫌抄袭侵权/违法违规的内容,侵犯到您的权益,请在线联系站长,一经查实,本站将立刻删除。 本文来自网络,若有侵权,请联系删除,如若转载,请注明出处:https://haidsoft.com/151456.html