大家好,欢迎来到IT知识分享网。
第一章 基本概念及定义
1-5 工质的状态变化过程
准平衡过程(准静态过程):过程进行得相对缓慢,工质有足够得时间来恢复平衡,随时都不致显著偏离平衡状态,这样的过程称为准平衡过程。相对弛豫时间来说,准平衡过程是进行得无限缓慢得过程,又称为准静态过程
因摩擦等造成机械功转变成热得现象称为耗散效应,类似得耗散现象还有电热效应等
可逆过程:当完成了某一过程之后,如果有可能使工质沿相同的路径逆行而恢复到原来状态,并使相互作用中所涉及的外界也恢复到原来状态,而不留下任何改变,这一过程称为可逆过程
一个可逆过程首先是准平衡过程,同时在过程中没有任何耗散效应
准平衡过程和可逆过程的区别:准平衡过程进行时可能发生能量耗散,可逆过程进行时不存在任何能量的耗散。可逆过程一定是准平衡过程,准平衡过程只是可逆过程的必要条件,可逆过程也可以用状态参数图上的连续实线表示
1-6 过程功和热量
功:在力学中把力和沿力方向位移的乘积定义为力所作的功;在热力学中功是热力系统通过边界而传递的能量,且其全部效果可表现为举起重物
热力学中约定系统对外界作功取为正,外界对系统作功取为负,单位为焦耳J,
比功:单位质量的物质所作的功,单位
功率:单位时间内完成的功,单位为瓦W,
膨胀功:
功的数值不仅取决于工质的初态和终态,还与过程的中间途径有关,功不是状态参数是过程量,
体积变化功:膨胀功或压缩功都是通过工质体积变化而与外界交换的功,统称体积变化功
体积变化功只与气体的压力和体积的变化量有关,和形状无关,且过程可逆
有用功(可以被利用的功)

可逆过程,
在无摩擦损失的理想情况下,功可以完全转为机械能,从这个意义上说功和机械能是等价的
系统和外界交换的功除体积变化功外还有固体中弹性力所作的功、液体表面张力所作的功、电极化功、磁化功等,
状态法则(状态公理):系统的独立状态参数数目N,等于系统对外所作的广义功数目n加1
简单可压缩系统和外界只交换一种形式功,独立的状态参数数目为2
热量:热力系与外界之间由于温度不同而通过边界传递的能量,单位焦耳J
工程热力学中约定:体系吸热,热量为正,反之,为负
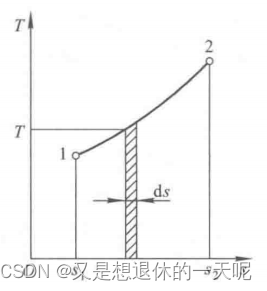
系统在可逆过程中与外界交换的热量
作功的过程中往往伴随着能量形态的转变,机械能转化为热能的过程可以由摩擦、碰撞等来完成,但只有通过工质压缩作功的转化过程才有可能可逆
功和热量的关系:热量和功都是能量传递的度量,是过程量。不同:功是有规则的宏观运动能量的传递,作功过程中往往伴随着能量形态的转化;热量则是大量微观粒子杂乱热运动的能量的传递,传热过程中不出现能量形式地转化;功转变成热量是无条件的,而热转变成功是有条件的
1-7 热力循环
热力循环:工质在经历了一系列状态变化过程后回到原来状态,这一系列过程的综合称为热力循环
全部由可逆过程组成的循环称为可逆循环,若循环中有部分过程或全部过程是不可逆的,则该循环为不可逆循环
在状态参数的平面坐标图上,可逆循环的全部过程构成一条闭合曲线
如果循环中系统内部的耗散效应可以忽略不计,但工质与热源的传热过程存在很大的不可逆性,不能忽略。此时,可以设想在工质与热源发生传热时有一个假想的物体处于其间,此假想物体与工质的温差无限小,即该传热过程是可逆的。这样,工质的循环就可看成是可逆循环,便于进行分析、讨论,这样的循环称为内可逆循环
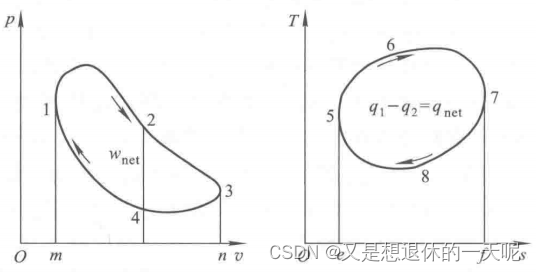
正向循环:将热能转化为机械能的循环,使外界得到功
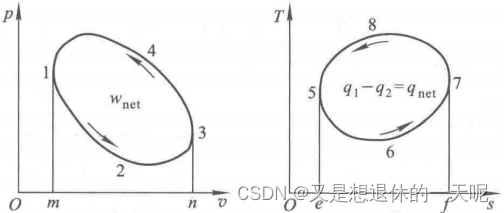
逆向循环:将热量从低温热源传给高温热源的循环,一般消耗外功
循环经济性指标的原则性定义:经济性指标=得到的收获/花费的代价
正向循环也称热动力循环,工质完成一个循环之后,对外作出正的净功,所以膨胀过程线的位置高于压缩过程线,膨胀功数值上大于压缩功。为此,可使工质在膨胀过程开始前或在膨胀过程中与高温热源接触,从中吸入热量;而在压缩过程开始前或在压缩过程中与低温热源接触,放出热量。这样就保证了在相同体积时膨胀过程的温度较压缩过程高,使得膨胀过程压力比压缩过程高,做到膨胀过程线位于压缩过程线之上
循环净功
热效率
逆向循环主要用于制冷装置和热泵,逆向循环时,工质在吸热前可先进行膨胀降温过程(如绝热膨胀),使工质的温度降低到能自低温热源吸取热量;而在放热过程前进行压缩升温过程(如绝热压缩),使其温度升高到能向高温热源放热
制冷系数
本章归纳
状态参数只是状态的函数,与如何达到指定状态的中间过程无关,因而可以建立起不论过程是否可逆,只要初、终态相同,其变化量就相同,进行循环后状态参数必定恢复到原值
区分开口系和闭口系的关键在于是否有质量越过边界而不在于系统内质量是否改变;绝热系的关键在于与外界没有热量交换,所以会有绝热的开口系;孤立系则与外界没有任何质、能的交换,因此系统及外界组成的复合系统就构成孤立系
系统平衡和稳定的差别是前者在没有外界作用的条件下仍能保持系统参数不随时间而改变,后者则是依赖外界的作用才维持系统参数不变
进行可逆过程与不可逆过程后系统都可以再恢复原来状态,但进行可逆过程后恢复原来状态可以不在外界留下任何影响,而不可逆过程后恢复原态必定在外界留下不可逆转的影响;可逆过程可在状态参数图上用实线表示其经历的无数个平衡状态,不可逆过程在状态参数图上只能标示过程中可能存在的若干平衡状态,故而只能用虚线示意;无论过程是否可逆,过程的热量和体积功都是过程量,除与系统初、终状态有关,还与经历的过程有关,但可逆过程的功和热量可分别用压容(p-v)图和温熵(T-s)图上过程线与横轴包围的面积表示,而不可逆过程的示意虚线下的面积没有实质意义
免责声明:本站所有文章内容,图片,视频等均是来源于用户投稿和互联网及文摘转载整编而成,不代表本站观点,不承担相关法律责任。其著作权各归其原作者或其出版社所有。如发现本站有涉嫌抄袭侵权/违法违规的内容,侵犯到您的权益,请在线联系站长,一经查实,本站将立刻删除。 本文来自网络,若有侵权,请联系删除,如若转载,请注明出处:https://haidsoft.com/157666.html