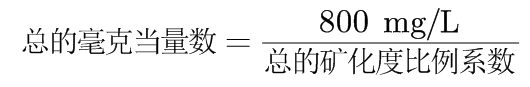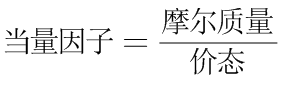大家好,欢迎来到IT知识分享网。
我现在是有每种离子的毫克当量百分数, 总的矿化度是800mg/L,以下是计算每种离子的质量浓度mg/L的计算步骤。严格按照以下计算步骤帮我写个MATLAB代码
1.计算总的毫克当量数(meq/L):
2. 计算每种离子的毫克当量数(meq/L):
3. 将每种离子的毫克当量数转换为质量浓度(mg/L):
首先,我们需要确定每种离子的摩尔质量和价态,以计算当量因子:
– Cl⁻: 摩尔质量 = 35.45 g/mol,价态 = 1
– SO₄²⁻: 摩尔质量 = 96.06 g/mol,价态 = 2
– HCO₃⁻: 摩尔质量 = 61.01 g/mol,价态 = 1
– Ca²⁺: 摩尔质量 = 40.08 g/mol,价态 = 2
– Na⁺: 摩尔质量 = 22.99 g/mol,价态 = 1
– Mg²⁺: 摩尔质量 = 24.31 g/mol,价态 = 2
计算每种离子的当量因子:
然后,利用这些当量因子计算每种离子的质量浓度:
1. 计算每种离子的质量浓度(mg/L):
– Cl⁻:
– SO₄²⁻:
– HCO₃⁻:
– Ca²⁺:
– Na⁺:
– Mg²⁺:
现在,让我们进行具体计算:
1. 计算总的毫克当量数:
– 我们先假设总的毫克当量数为 X meq/L。
– 则每种离子的毫克当量数:
– Cl⁻: \( 0.53X \) meq/L
– SO₄²⁻: \( 0.37X \) meq/L
– HCO₃⁻: \( 0.10X \) meq/L
– Ca²⁺: \( 0.64X \) meq/L
– Na⁺: \( 0.19X \) meq/L
– Mg²⁺: \( 0.16X \) meq/L
2. 求总的质量浓度:
–
3. 解方程:
4. 计算每种离子的质量浓度:
– Cl⁻:
– SO₄²⁻:
– HCO₃⁻:
– Ca²⁺:
– Na⁺:
– Mg²⁺:
结果如下:
– Cl⁻: 243.25 mg/L
– SO₄²⁻: 230.59 mg/L
– HCO₃⁻: 79.00 mg/L
– Ca²⁺: 165.90 mg/L
– Na⁺: 56.38 mg/L
– Mg²⁺: 25.16 mg/L
免责声明:本站所有文章内容,图片,视频等均是来源于用户投稿和互联网及文摘转载整编而成,不代表本站观点,不承担相关法律责任。其著作权各归其原作者或其出版社所有。如发现本站有涉嫌抄袭侵权/违法违规的内容,侵犯到您的权益,请在线联系站长,一经查实,本站将立刻删除。 本文来自网络,若有侵权,请联系删除,如若转载,请注明出处:https://haidsoft.com/141657.html